高分期刊认证的纳米检测技术:ApogeeFlow纳米流式仪推动放疗副作用机制突破
国际代谢领域高分期刊《Cell Metabolism》最新发表的研究中,武汉大学生命科学学院的科学家首次揭示肿瘤细胞通过细胞外囊泡(EVs)介导放疗后肌肉纤维化的分子机制。该研究通过ApogeeFlow A60 Micro PLUS纳米流式仪实现EVs分泌动态的精准量化,为关键病理机制的发现提供了不可替代的实验证据。
高影响力期刊背书的方法学严谨性
在闫卫教授组的研究人员构建的多组学研究中,纳米流式检测技术被整合入标准化实验流程。研究团队使用ApogeeFlow系统对肿瘤源性EVs进行绝对定量分析(论文中STAR Methods章节),发现接受放疗的小鼠乳腺癌模型(4T1/Ctrl-RT)分泌的EVs数量较对照组显著提升。该数据直接证实了"放疗触发肿瘤EVs超量分泌"的核心假设,为后续机制探索奠定基础。这种方法学设计通过Cell Metabolism的评审,彰显了纳米流式技术在复杂生物系统研究中的可靠性。
定量数据驱动药物机制解析
当研究推进至治疗策略验证阶段,ApogeeFlow提供的客观数据成为区分药物作用机制的关键。实验显示:外泌体分泌抑制剂GW4869显著降低EVs数量,而抗纤维化药物Losartan对EVs分泌无显著影响(图1)。这种量化差异精准揭示了Losartan通过阻断SRM蛋白修饰而非抑制EVs释放来缓解肌肉损伤的作用模式,为其临床应用方向提供了理论依据。
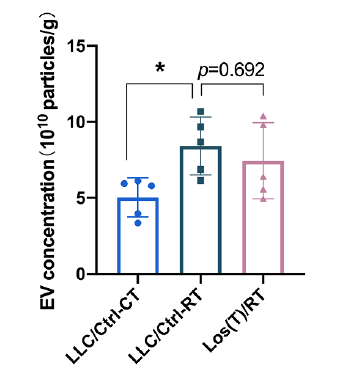
图1
从动物模型到临床样本的转化验证
研究进一步利用该技术分析癌症患者血浆样本,发现乳腺癌与肺癌患者放疗后血浆EVs粒径分布向>80 nm偏移,而结直肠癌患者未见此现象。该发现与动物模型数据形成相互印证,揭示了肿瘤类型特异性的EVs分泌规律。
技术参数的科学适配性
本研究所采用的ApogeeFlow A60 Micro PLUS系统,其检测范围精准覆盖肿瘤分泌的主要EVs亚群。通过NIST可追溯标准品(批号#1493/#1426)校准设备,确保定量数据可比性。这些方法论细节均被纳入Cell Metabolism的补充材料,体现了顶级期刊对技术严谨性的要求。
该研究不仅为放疗副作用提供了新干预靶点,更确立了纳米流式技术在肿瘤微环境研究中的方法论地位。基于高分影响因子期刊的严格审阅,ApogeeFlow系统在转化医学研究中的价值获得认证。

广州进科驰安科技有限公司
Bio-Gene Technology Ltd.
热线:176 2009 3784
www.bio-gene.com.cn
marketing@bio-gene.com.cn
香港 北京 上海 广州








 药物筛选/分子生物学
药物筛选/分子生物学